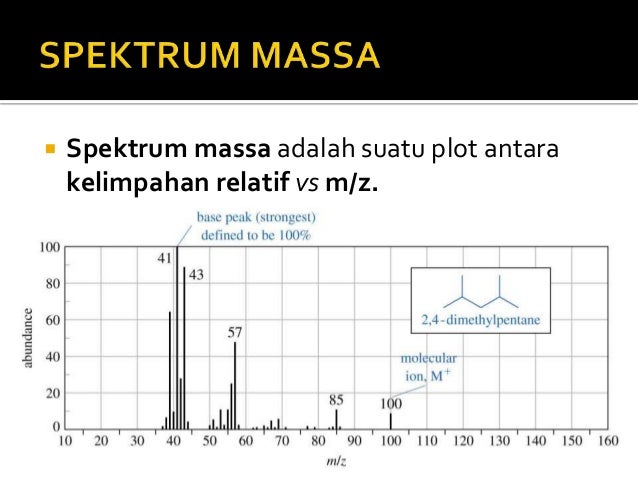
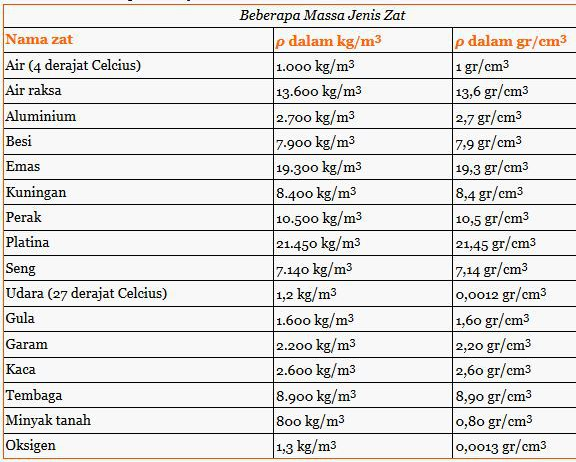
60 90 Massa
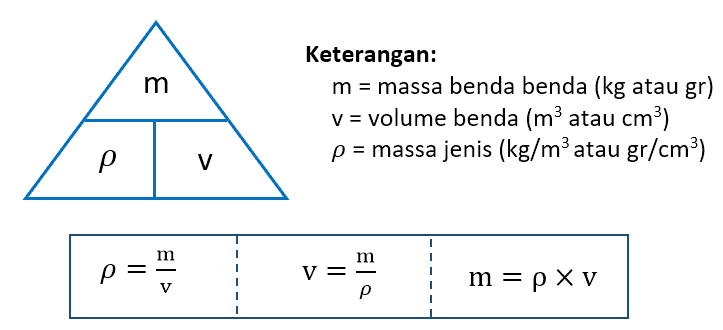
Molalitas 10 x 1000 1 899 1 9 m.
60 90 massa. Contoh perhitungan molalitas larutan. Aku sekarang kelas 6 tryout kemarin aku rangking 1. N h 2 o 90 18 5 mol. Gunakan kecerdasan ribuan ahli dan pakar di seluruh dunia.
O 18 02 g mol e 1 60 x 10 19 c 1 v 1 kg m2 s2 c prinsip ms. Massa ms prinsip dan instrumentasi prinsip ms. Berat dituliskan dalam kgf. Massa air yang volumenya sama 24.
Memilah ion molekul dalam fase gas dari inlet diionisasi oleh berkas. Misalnya 10 gram natrium hidroksida naoh dilarutkan. Jadi jika anda mendapatkan satuan tersebut anda telah mengerjakan soal dengan benar. Jumlah mol urea n gram mr 3 60 0 05 mol molaritas larutan m n v 0 05 0 25 0 2 molar maka molaritas larutan urea yaitu 0 2 molar atau 0 2 mol liter.
Jadi fraksi mol urea co nh 2 2 yang dibuat dengan melarutkan 30 gr urea ke dalam 90 gram air sebesar 0 09. Jadi massa jenis relatif dari zat cair tersebut ialah 1 2. Jika terdapat 17 gram suatu oksida logam dengan rumus empiris m2o3 mempunyai kandungan 8 gram oksigen. Newton adalah satuan si.
Massa jenis relatif massa zat cair. Massa 90 newton m s 2 massa 90 kg m s 2 m s 2 sederhanakan satuan massa 90 kg. Ch2o n 90 1 ar c 2. Konsentrasi larutan asam formiat hcooh 4 6 massa dengan massa jenis 1 01 g ml adalah mr chooh 46.
Larutan nacl 10 massa berarti dalam 100 gram larutan nacl terdapat nacl murni sebanyak 10 x 100 gram 10 gram. Sehingga rumus molekul senyawanya ialah c3h6o3. Massa jenis atau densitas adalah suatu besaran kerapatan massa benda yang dinyatakan dalam berat benda per satuan volume benda tersebut. Ar o n 90 1.
Massa air sebagai pelarut 100 10 gram 90 gram. Memilah ion lintasan lengkung r ion tergantung pada b. Molaritas larutan urea bisa dihitung dengan cara. Massa h 2 o 90 gr.
Brainly belajar jadi luar biasa terima kasih brainly rusi hastarii. Besaran massa jenis dapat membantu menerangkan mengapa benda yang berukuran sama memiliki berat yang berbeda. Jika ar o sebesar 16. Massa zat cair 90 70 24 g massa botol sarat air 90 g massa air yang volumenya sama 90 70 20 g.
Berapa fraksi mol pelarut yang dibuat dengan melarutkan 90 gram glukosa mr 180 dalam 90 gram air mr 18. N co nh 2 2 30 60 0 5 mol. Kg adalah satuan massa yang tepat. 90 atau 60o prinsip ms.
Ar h 1. Massa o 8 gram. Terima kasih brainly nilaiku yg tadi juga jelek 60 50 40 sekarang matematika jadi 100 99 98 wah kerren.